Adakveo مقابل Oxbryta: التعرف على بدائل crizanlizumab الخاصة بك
آخر تحديث 15 كانون الثاني/يناير 2024
يمكنك الحصول على الأدوية الجديدة بشكل قانوني، حتى لو لم تتم الموافقة عليها في بلدك.
تعلّم كيف
بعد إلغاء ترخيص عقار Adakveo crizanlizumab) في الاتحاد الأوروبي، يحتاج العديد من المرضى والأطباء إلى إيجاد بديل لدواء Adakveo .
إذا كانت استجابتك للعلاج جيدة، فلا يزال بإمكانك الحصول على Adakveo حتى لو لم يعد معتمداً في الاتحاد الأوروبي. ومع ذلك، إذا كان طبيبك يفضل تغيير مسار علاجك، فمن الجيد أن تفهم ما يعنيه ذلك بالنسبة لك كمريض.
في هذه المقالة سنلقي نظرة على أحد بدائل Adakveo المحتملة التي قد يرغب طبيبك في مناقشتها - Oxbryta voxelotor). ستجد هنا نظرة عامة سريعة على أوجه التشابه والاختلاف بين Adakveo Oxbryta.
Adakveo مقابل Oxbryta: ما الغرض من استخدامهما؟
كل من Adakveo Oxbryta هما دواءان يُصرفان بوصفة طبية لعلاج داء فقر الدم المنجلي 1،2. ومع ذلك، يستهدف كل من الدواءين جانبًا مختلفًا من جوانب المرض.
يهدف Adakveo إلى تقليل تواتر نوبات انسداد الأوعية الدموية المؤلمة، في حين يستخدم Oxbryta لعلاج فقر الدم الانحلالي لدى مرضى فقر الدم المنجلي 1،2.
في أي عمر تمت الموافقة على Oxbryta في الاتحاد الأوروبي؟
على عكس Adakveo الذي لا يمكن استخدامه إلا للمرضى الذين تبلغ أعمارهم 16 عامًا فأكثر، فإن Oxbryta موصوف أيضًا للمرضى الأطفال.
في الولايات المتحدة الأمريكية، يمكن وصف Oxbryta اعتبارًا من سن 4 سنوات، بينما في الاتحاد الأوروبي، لا تتم الموافقة على استخدام الأطفال إلا من سن 12 عامًا 1،2.
Crizanlizumab مقابل Voxelotor: كيف يعملان؟
بينما يهدف كلا الدواءين إلى الحد من مضاعفات داء فقر الدم المنجلي، إلا أنهما يستهدفان جوانب مختلفة من المرض.
Adakveo والحد من الأزمات المؤلمة
يهدف Adakveo إلى تقليل تكرار الأزمات المؤلمة، والتي تحدث عندما تعلق خلايا الدم المشوهة في الأوعية الدموية.
المكون النشط للدواء، crizanlizumab هو نوع معين من البروتين يُعرف باسم الجسم المضاد أحادي النسيلة. صُمم هذا البروتين ليرتبط بمادة P-selectin، وهي مادة موجودة على الطبقة الخارجية للخلايا المبطنة للأوعية الدموية.
يساعد بروتين P-selectin الخلايا على الالتصاق بالأوعية الدموية ويشارك في انسداد الأوعية الدموية أثناء النوبات المؤلمة في مرض فقر الدم المنجلي. ومن خلال الاتصال بدواء P-selectin وتثبيط وظيفته، يهدف دواء Adakveo إلى منع هذه النوبات المؤلمة 3.
Oxbryta والوقاية من فقر الدم (الأنيميا)
من ناحية أخرى، يهدف Oxbryta إلى الوقاية من فقر الدم المرتبط بداء فقر الدم المنجلي.
يعمل العنصر النشط في Oxbryta voxelotor على تعزيز قدرة الهيموغلوبين على الاحتفاظ بالأكسجين ويمنعه من تكوين سلاسل متصلبة داخل الأوعية الدموية. وهذا يساعد خلايا الدم الحمراء في الحفاظ على شكلها الطبيعي ومرونتها. كما أنه يقلل من معدل تدميرها المبكر ويطيل عمرها 4.
ما مدى كفاءة Adakveo Oxbryta
تمت دراسة فعالية عقار Adakveo crizanlizumab) Oxbryta voxelotor) في التجارب السريرية.
-
نتائج التجارب السريرية Adakveo
استندت موافقة إدارة الغذاء Adakveo الأمريكية (FDA)، وكذلك ترخيص تسويقه المبدئي في الاتحاد الأوروبي على نتائج الدراسة السريرية SUSTAIN. وقارنت الدراسة بين Adakveo (مع أو بدون هيدوكسي يوريا) ضد العلاج الوهمي.
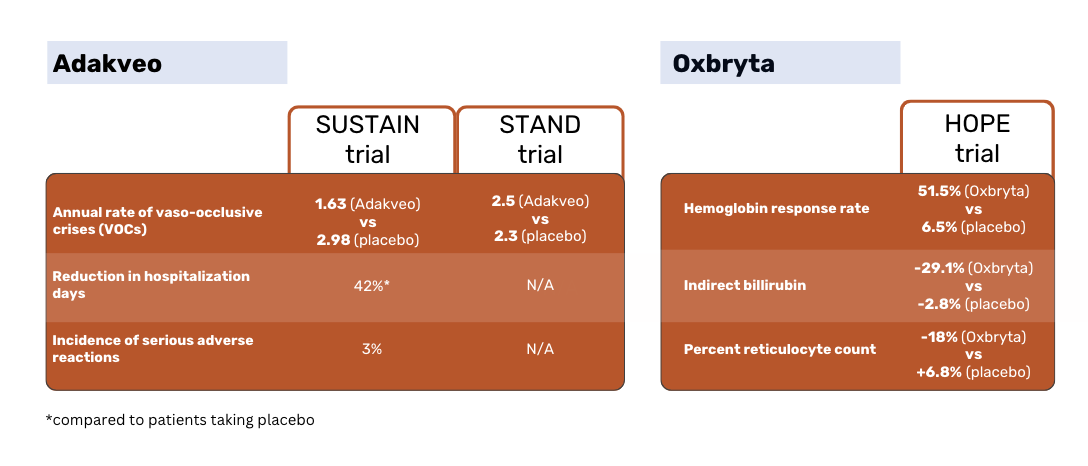
وفقًا لنتائج دراسة SUSTAIN، كان لدى المرضى الذين عولجوا بعقار Adakveo معدل سنوي أقل من الناحية الإحصائية من حيث متوسط معدل الأزمات الوعائية الانسدادية الوعائية (VOCs) - 1.63 مقابل 2.98 للمرضى الذين تناولوا العلاج الوهمي. لم يتعرض 36% من مرضى Adakveo في التجربة لأي أزمات انسداد وعائي وعائي خلال فترة التجربة التي استمرت 52 أسبوعًا، مقارنة ب 17% من مرضى العلاج الوهمي 1.
ما هي نتائج تجربة Adakveo ستاند؟
فشلت دراسة المرحلة الثالثة العالمية STAND، التي قارنت مرة أخرى بين Adakveo والعلاج الوهمي، في إظهار فرق ذي دلالة إحصائية في معدل النوبات المؤلمة بين مجموعات المرضى. عانى المرضى الذين عولجوا بعقار Adakveo في المتوسط 2.5 نوبة مؤلمة خلال عام من العلاج - لا تختلف بشكل كبير عن 2.3 نوبة في المتوسط في مجموعة العلاج الوهمي 3.
أصبحت النتائج غير المقنعة لتجربة STAND أساسًا لإلغاءAdakveo في الاتحاد الأوروبي.
-
نتائج تجارب Oxbryta السريرية
في تجربة HOPE، تم اختبار Oxbryta مقابل العلاج الوهمي. استندت الفعالية إلى معدلات استجابة الهيموجلوبين (Hb) التي تم تعريفها على أنها زيادة في الهيموجلوبين بنسبة > 1 جم/ديسيلتر من خط الأساس إلى الأسبوع 24.
بلغت نسبة الاستجابة لدى مرضى Oxbryta 51.1% مقابل 6.5% لدى مرضى العلاج الوهمي. انخفضت نسبة البيليروبين غير المباشر بنسبة 29.1% لدى مرضى Oxbryta مقابل انخفاض بنسبة 2.8% لدى المرضى الذين يتناولون العلاج الوهمي. انخفضت النسبة المئوية لتعداد الخلايا الشبكية بنسبة 18% لدى مرضى Oxbryta وزادت بنسبة 6.8& لدى مرضى العلاج الوهمي 2.
كما تُظهر البيانات المشتركة، لا يمكن إجراء مقارنة مباشرة بين الدواءين، حيث تم استخدام معايير فعالية مختلفة في التجارب السريرية الخاصة بهما. نظرًا لأن كلا العلاجين يتعاملان مع داء فقر الدم المنجلي بطريقة مختلفة، فمن المحتمل ألا يكون Oxbryta بديلاً مباشرًا Adakveo بل جزءًا من خطة علاجية جديدة سيضعها طبيبك لك.

Adakveo مقابل Oxbryta: السلامة والآثار الجانبية
وفقًا لمعلومات الوصفة الطبية، هذه هي الآثار الجانبية الأكثر شيوعًا Adakveo Oxbryta:
الآثار الجانبية Adakveo
- الغثيان
- آلام المفاصل
- آلام الظهر
- ألم المعدة
- الحمى1.
خلال تجربة SUSTAIN، عانى 3% من المرضى من تفاعلات مرتبطة بالتسريب، والتي تتميز بأعراض مثل الصداع أو القشعريرة أو القيء أو الإسهال أو ضيق التنفس أو الصفير 1.
الآثار الجانبية Oxbryta
- الصداع
- الإسهال
- ألم المعدة
- الغثيان
- الطفح الجلدي
- الحمى 2.
عانى أقل من 1% من مرضى التجارب السريرية من تفاعلات فرط الحساسية الخطيرة بما في ذلك الطفح الجلدي وضيق التنفس الخفيف وتورم خفيف في الوجه وكثرة الحمضات (زيادة في عدد خلايا الدم البيضاء)2.
Adakveo مقابل Oxbryta: مقارنة الأسعار
عندما يتعلق الأمر بأسعار الأدوية التي لم يتم اعتمادها أو إتاحتها بعد، يجب أن تعتبرها إرشادية فقط. قد يختلف السعر النهائي حسب موقعك أو المورد.
تكاليف Adakveo في السنة
الجرعة الموصى بها Adakveo هي 5 ملغم/كغم من كتلة الجسم كل 4 أسابيع. وهذا يعني 13 حقنة في السنة. بالنسبة للشخص الذي يزن 60 كجم، سيتطلب ذلك 13 حقنة ضخ × 300 مجم من Adakveo أو 39 قارورة من الدواء.
وبسعر حوالي 5,214 يورو لكل 100 مجم للقارورة الواحدة، فإن التكلفة السنوية لعلاج Adakveo تصل إلى حوالي 203,346 5 يورو.
تكاليف Oxbryta في السنة
الجرعة الموصى بها من Oxbryta للمرضى الذين يزيد وزن جسمهم عن 40 كجم هي 1,500 مجم من Oxbryta مرة واحدة يومياً، أي ما يعادل 3 أقراص × 500 مجم لكل منها.
تبلغ تكلفة علبة 90 قرص × 500 مجم حوالي 40,365 يورو، وتكفي لمدة شهر واحد، بناءً على الجرعة الموصى بها أعلاه. وبالتالي، فإن التكلفة السنوية لعلاج Oxbryta تصل إلى 484,380 6 يورو.
أين تمت الموافقة على Adakveo Oxbryta
تمت الموافقة على دواء Adakveo crizanlizumab) حاليًا في العديد من البلدان، بما في ذلك الولايات المتحدة الأمريكية وكندا وأستراليا 7،9،10. تم إلغاء ترخيص تسويقه المشروط في الاتحاد الأوروبي في مايو 2023 3.
تمت الموافقة على Oxbryta voxelotor) في الولايات المتحدة الأمريكية والاتحاد الأوروبي وكندا 4،8،9. ومع ذلك، داخل الاتحاد الأوروبي، لم يتوفر Oxbryta بعد على نطاق واسع في السوق، حيث يمكن أن يختلف الوقت بين الترخيص وطرحه في السوق بشكل كبير من بلد لآخر.
هل Adakveo أو Oxbryta غير معتمد (بعد الآن) أو متاح في بلدك؟ إذا كنت ترى أنت وطبيبك أن هذه العلاجات قد تفيدك، فتواصل مع فريق خبراء الوصول إلى الأدوية لدينا. يمكننا أن نقدم لك عرض أسعار مخصص لتوفير الدواء لك.
المراجع:
- أبرز معلومات الوصفة الطبية. نوفارتيس، تم الوصول إليه في 27 سبتمبر 2023.
- أبرز معلومات الوصفة الطبية. Oxbryta تم الوصول إليه في 27 سبتمبر 2023.
- Adakveo | الوكالة الأوروبية للأدوية. وكالة الأدوية الأوروبية، تم الوصول إليه في 27 سبتمبر 2023.
- Oxbryta | وكالة الأدوية الأوروبية. وكالة الأدوية الأوروبية، تم الوصول إليه في 27 سبتمبر 2023.
- اشتر Adakveo (crizanlizumab) عبر الإنترنت. Everyone.org تم الوصول إليه في 27 سبتمبر 2023.
- اشتر Oxbryta (voxelotor) عبر الإنترنت. Everyone.org تم الوصول إليه في 27 سبتمبر 2023.
- Adakveo. إدارة السلع العلاجية (TGA)، تم الوصول إليه في 27 سبتمبر 2023.
- إدارة الغذاء والدواء الأمريكية توافق على دواء لعلاج مرض فقر الدم المنجلي لدى الأطفال إدارة الغذاء والدواء، 17 ديسمبر 2021.
- الأدوية الجديدة المعتمدة في عام 2019 - مراقبة دخول الأدوية. Canada.ca، 10 فبراير 2021.
- إدارة الغذاء والدواء الأمريكية توافق على أول علاج موجه لعلاج المرضى الذين يعانون من مضاعفات مؤلمة لمرض فقر الدم المنجلي إدارة الغذاء والدواء، 15 نوفمبر 2019.