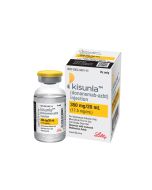
الموافقة على دونانماب حول العالم: إلى متى ستنتظر؟
آخر تحديث 04 ديسمبر 2024

يمكنك الحصول على الأدوية الجديدة بشكل قانوني، حتى لو لم تتم الموافقة عليها في بلدك.
تعلم كيفبعد أن أوقفت إدارة الغذاء والدواء الأمريكية (FDA) في البداية العمل بدواء كيسونلا (دونانيماب) برفضها طلب الموافقة المعجلة عليه في عام 2023، انقلبت الأمور الآن 1. حصل دواء الزهايمر الجديد على موافقة إدارة الغذاء والدواء الأمريكية في يوليو 2024 بعد أن أوصت مجموعة من الخبراء المستقلين بالموافقة عليه في يونيو 2024 2.
بالنسبة لمرضى ألزهايمر المبكر في كل مكان، هذه علامة أمل. ولكن ما هي الجداول الزمنية للموافقة التي تواجهها إذا كنت في أوروبا أو المملكة المتحدة أو أي مكان آخر؟ إليك كل ما تحتاج إلى معرفته.
دونانيماب: دواء الزهايمر الجديد الذي يبعث الأمل في مرضى الزهايمر
على غرار دواء ليكيمبي (ليكانماب) ودواء Aduhelm (أدوكانوماب) اللذين تمت الموافقة عليهما سابقًا، يعمل كيسونلا (دونانيماب) أيضًا من خلال استهداف لويحات الأميلويد في الدماغ. يرتبط تراكم هذه اللويحات بأعراض مرض الزهايمر. وتهدف إزالتها إلى إبطاء تقدم التدهور المعرفي.
دونانيماب مقابل ليكانيماب
هناك اختلافان رئيسيان بين دونانيماب وسابقه ليكيمبي (ليكانيماب):
- تكرار الحقن الوريدي: يتطلب ليكانماب الحقن الوريدي مرة كل أسبوعين، بينما يتم إعطاء دونانيماب مرة كل 4 أسابيع;
- طرق مختلفة لاستهداف لويحات أميلويد بيتا: بينما يستهدف عقار ليكانيماب لويحات الأميلويد عندما تبدأ في تكوين ألياف، يرتبط دونانيماب بها بعد أن تكون قد تكتلت بالفعل 3.
ما هو معدل نجاح الدونانيماب في التجارب السريرية؟
في المرحلة الثالثة من التجربة السريرية TRAILBLAZER-ALZ 2، تم استخدام عقار دونانيماب في المرضى الذين يعانون من الأعراض المبكرة لمرض الزهايمر 4. وتشمل بعض النتائج الرئيسية التي تم الإبلاغ عنها ما يلي:
- كان هناك تباطؤ بنسبة 35% في التدهور المعرفي لدى المرضى الذين يعانون من مستوى متوسط من تاو وأعراض سريرية لمرض الزهايمر. وعلى مدار 18 شهرًا، كان تباطؤ التدهور بنسبة 36%;
- لم يشهد 47% من المرضى الذين عولجوا بدواء دونانيماب أي انخفاض في مقياس CDR-SB بعد عام واحد من بدء التجربة. في مجموعة العلاج الوهمي، لم يشهد 29% من المرضى أي انخفاض في مقياس CDR-SB;
- 52% من مرضى الدونانماب أكملوا علاجهم في غضون عام واحد و72% - في غضون 18 شهرًا، نتيجة لتطهير اللويحات;
- كان لدى المرضى الذين عولجوا بالدونانيماب انخفاض أقل بنسبة 40% في أداء المهام اليومية عند نقطة التحقق التي استمرت 18 شهرًا;
- كان المرضى الذين يتلقون الدونانماب أقل عرضة بنسبة 39% لتطور المرض إلى المرحلة التالية من المرض 4.
طريق دونانيماب إلى موافقة إدارة الغذاء والدواء الأمريكية: ما هو الوضع؟
مع التوصية الإيجابية التي قدمها الخبراء المستقلون في يونيو 2024، تم تمهيد الطريق للحصول على موافقة إدارة الغذاء والدواء الأمريكية على الدونانيماب. في 2 يوليو 2024، حصل كيسونلا (دونانيماب) رسميًا على موافقة إدارة الغذاء والدواء الأمريكية 11.
متى سيحصل دونانيماب على موافقة EMA؟
لا يزال طلب ترخيص تسويق دونانيماب في الاتحاد الأوروبي قيد المراجعة منذ أغسطس 2023. وعادةً ما تستغرق عملية موافقة الاتحاد الأوروبي ما يصل إلى 210 أيام، ولكن في هذه الحالة، تستغرق وقتًا أطول. من الممكن نظريًا أن تتم الموافقة على دونانيماب في أوروبا خلال عام 2024. ومع ذلك، وبالنظر إلى التأخير في الموافقة على سلفه Leqembi الذي لا يزال يعاني من التأخير، فمن المستحيل التنبؤ بالجدول الزمني.
متى سيتوفر دونانيماب في أوروبا؟
إذا افترضنا السيناريو الأفضل، وهو أن يحصل دونانيماب على الموافقة الأوروبية قبل نهاية عام 2024، فهذا لا يعني أنه سيصبح متاحًا في جميع أنحاء أوروبا في الوقت نفسه.
لكل دولة عضو في الاتحاد الأوروبي عمليتها المحلية الخاصة بها وجدولها الزمني لطرح الأدوية المعتمدة حديثًا. يبلغ المتوسط في الاتحاد الأوروبي 511 يومًا، حيث تعد ألمانيا الأسرع (133 يومًا) ورومانيا الأبطأ (899 يومًا) 5.
وبعبارة أخرى، حتى بالنظر إلى أفضل السيناريوهات، فإن أقرب وقت يمكن أن توفر فيه بعض البلدان في أوروبا دونانماب هو منتصف عام 2025. قد يواجه المرضى في بلدان أخرى أكثر من عامين من وقت الانتظار الإضافي.
هل موافقة هيئة تنظيم الموارد البشرية البريطانية (MHRA) على الدونانيماب؟
نعم، ومنذ أكتوبر 2024، هذه حقيقة واقعة.
متى سيتوفر دونانيماب في المملكة المتحدة؟
بينما تمت الموافقة على استخدام دونانيماب بالفعل في المملكة المتحدة، فإن هذا لا يعني أنه متاح في هيئة الخدمات الصحية الوطنية بعد. لا يزال المعهد الوطني للصحة والتقييم (NICE) يقيّم الدواء، ومن المتوقع أن يصدر قرار في مارس 2025. إذا كانت النتيجة إيجابية، فمن المفترض أن يكون دونانيماب متاحًا في هيئة الخدمات الصحية الوطنية في غضون 3 أشهر من قرار المعهد الوطني للصحة العامة (أي حوالي منتصف عام 2025).
متى سيتوفر دونانيماب في البلدان الأخرى؟
يجري تقييم دونانيماب للموافقة عليه في العديد من البلدان الأخرى، بما في ذلك:
- أستراليا: تقوم هيئة الدواء الأسترالية بمراجعة طلب دونانيماب منذ أكتوبر 2023 6. تستغرق عملية الموافقة الأسترالية ما يصل إلى 330 يومًا، مما يعني أنه يمكن نظريًا الموافقة على دونانيماب في حوالي سبتمبر 2024.
- كندا: يجري النظر أيضًا في الحصول على الموافقة على دونانيماب في كندا (قيد المراجعة منذ فبراير 2024) 7. يمكن أن تستغرق قرارات الموافقة من قبل وزارة الصحة الكندية ما بين 7 أشهر وسنة واحدة، مما يعني أن دونانيماب يمكن أن يحصل نظريًا على الموافقة في كندا في أوائل عام 2025.
- الصين: في نوفمبر 2023، قدمت شركة Eli Lilly طلب الموافقة على عقار دونانيماب إلى هيئة الدواء الصينية في الصين. وقد تحسنت الجداول الزمنية للموافقة في الصين منذ إصلاحها التنظيمي لعام 2015، وهي الآن بمتوسط 6.8 أشهر 8. وهذا يعني أن هيئة الدواء الصينية قد توافق نظريًا على دونانيماب في منتصف عام 2024، مما قد يجعلها أول دولة تعطي الضوء الأخضر لدواء الزهايمر الجديد. سواء حدث ذلك أم لا، فالوقت وحده كفيل بإثبات ذلك.
- اليابان: اعتبارًا من سبتمبر 2024، تمت الموافقة على دونانيماب في اليابان 9.
ماذا لو استغرقت عملية الموافقة على الدواء في بلدك وقتاً طويلاً، أو كنت مقيماً في مكان لم تبدأ فيه عملية الموافقة على الدواء؟
كيفية الحصول على دونانيماب قبل الموافقة عليه في بلدك
هل أنت مريض بالزهايمر المبكر؟ إذا كان طبيبك يرى أنك قد تستفيد من العلاج بدواء دونانيماب، فقد لا تحتاج إلى انتظار الموافقة المحلية عليه. بدلاً من ذلك، يمكنك أنت وطبيبك التفكير في الانضمام إلى تجربة سريرية. أو، شراء دونانيماب والحصول عليه عن طريق استيراد المريض المسمى.
انضم إلى إحدى التجارب السريرية على الدونانماب
تتمثل إحدى طرق الحصول على دونانيماب في التسجيل في تجربة سريرية. قد يكون قول هذا الأمر أسهل من فعله في كثير من الأحيان، حيث ستحتاج أنت وطبيبك إلى العثور على تجربة تقوم حالياً بتجنيد مشاركين في بلدك. كما سيتعين عليك أيضاً استيفاء معايير الأهلية الخاصة بهم وقبول المخاطرة بأن يتم تعيينك في المجموعة الضابطة في التجربة.
فيما يلي بعض الأماكن الجيدة للبدء في البحث عن التجارب السريرية الجارية على الدونانماب:
- ClinicalTrials.gov: هذه قاعدة بيانات تضم جميع التجارب السريرية في الولايات المتحدة الأمريكية. بعض التجارب مفتوحة أيضاً للمشاركين الدوليين. من الأمثلة على ذلك التجربة السريرية TRAILBLAZER-ALZ 5 مع دونانيماب، وهي مفتوحة للمرضى في المملكة المتحدة والصين وأمريكا الجنوبية وبلدان أخرى 10.
- EUClinicaltrials.eu: هذه قاعدة بيانات تحتوي على جميع التجارب السريرية في الاتحاد الأوروبي. ويحتوي حاليا على معلومات محدودة عن التجارب التي بدأت قبل 31 كانون الثاني/يناير 2022. بالنسبة لتلك التجارب ، يمكنك الرجوع إلى سجل التجارب السريرية للاتحاد الأوروبي.
- myTomorrows: تدعم هذه المنظمة المرضى في إيجاد خيارات العلاج في التجارب السريرية.
اشتر دونانيماب عن طريق استيراد المرضى المسمين
في معظم البلدان، يُسمح للمرضى قانوناً بشراء واستيراد الأدوية التي يمكن أن تحسّن جودة حياتهم أو تعالج الحالات التي تهدد حياتهم. إذا كنت ترغب في الحصول على دواء دونانيماب قبل الموافقة عليه في بلدك، فقد يكون هذا خياراً متاحاً لك ولطبيبك.
تُعرف اللائحة التي تتيح ذلك باسم استيراد المريض المسمى. قد تكون هناك اختلافات بين البلدان من حيث المتطلبات الإدارية المحددة. ومع ذلك، يجب استيفاء هذه المعايير في جميع الحالات:
- الدواء المعني لديه موافقة السوق في بلد آخر ولم تتم الموافقة عليه (بعد) أو توفره في بلد المريض ؛
- لا يوجد بديل في السوق المحلية.
- الدواء للاستخدام الشخصي.
- لدى المريض وصفة طبية من الطبيب المعالج;
- يتحمل الطبيب مسؤولية العلاج. قد يتطلب ذلك وثائق مختلفة من بلد إلى آخر.
هل ترغب في استخدام لائحة استيراد المريض المسمى فرديًا للحصول على دونانيماب قبل موافقة الاتحاد الأوروبي عليه (أو الموافقة عليه في المملكة المتحدة أو الصين أو كندا أو اليابان أو أستراليا أو أي مكان آخر)؟ ستحتاج أولاً إلى استشارة طبيبك المعالج والحصول على وصفة طبية مناسبة.
هل لديك وصفة طبية بالفعل؟ يمكن لفريقنا دعمك في شراء دونانيماب أينما كنت. تواصل معنا لمزيد من المعلومات.
مراجع:
- بيسلي، د. إيلي ليلي تقول إن إدارة الأغذية والعقاقير الأمريكية ترفض الموافقة المعجلة على عقار الزهايمر. رويترز، 19 يناير 2023.
- دونانيماب: خبراء إدارة الغذاء والدواء الأمريكية يوصون بالموافقة على عقار الزهايمر. The BMJ، 14 يونيو 2024.
- ليكيمبي (ليكانماب) مقابل دونانيماب لمرض الزهايمر: ما الفرق بينهما؟ التسريب المحلي، تم الوصول إليه في 18 يونيو 2024.
- عقار دونانيماب من شركة ليلي يبطئ بشكل ملحوظ من التدهور المعرفي والوظيفي في المرحلة الثالثة من دراسة لمرض الزهايمر المبكر. Investors.lilly.com، تم الوصول إليه في 18 يونيو 2024.
- استبيان مؤشر المرضى EFPIA W.A.I.T. استبيان مؤشر 2021. EFPIA، تم الوصول إليه في 18 يونيو 2024.
- كيسونلا إيلي ليلي أستراليا المحدودة. إدارة السلع العلاجية (TGA)، تم الوصول إليه في 18 يونيو 2024.
- طلبات الأدوية والمنتجات الصحية قيد المراجعة (SUR). Canada.ca، تم الوصول إليه في 18 يونيو 2024.
- ديفيدسون، أ. وآخرون، الإصلاح التنظيمي في الصين: تحديث بشأن الجداول الزمنية للمراجعة وتأخر الأدوية. PPD، تم الوصول إليه في 18 يونيو 2024.
- تمت الموافقة على دواء كيسونلا™ (دونانيماب-أزبت) من ليلي في اليابان لعلاج مرض الزهايمر المبكر الأعراض. ليلي، تم الوصول إليه في 04 ديسمبر 2024.
- دراسة عن عقار دونانيماب (LY3002813) لدى المشاركين الذين يعانون من مرض الزهايمر المبكر الأعراض (TRAILBLAZER-ALZ 5). ClinicalTrials.gov، تم الوصول إليه في 18 يونيو 2024.
- إدارة الغذاء والدواء الأمريكية توافق على كيسونلا. Drugs.com، تم الوصول إليه في 03 يوليو 2024.