ما الفرق بين ليكيمبي Aduhelm نظرة عامة بسيطة.
آخر تحديث 19 نوفمبر 2024
يمكنك الحصول على الأدوية الجديدة بشكل قانوني، حتى لو لم تتم الموافقة عليها في بلدك.
تعلّم كيفمنذ عام 2021، منحت إدارة الغذاء والدواء الأمريكية (FDA) الموافقة المعجلة على دواءين جديدين من أدوية الزهايمر. وهذان الدواءان هما علاجا ليكيمبي (ليكانماب) Aduhelm (أدوكانوماب) المضادان للأميلويد. جاءت كلتا الموافقات بعد ما يقرب من 20 عامًا دون تحقيق اختراقات كبيرة في علاج الزهايمر. ولهذا السبب، حظي كلا الدواءين باهتمام إعلامي واسع النطاق.
ومع ذلك، كان الاستقبال متباينًا. فقد أشارت ماريا كارييو، كبيرة المسؤولين العلميين في جمعية الزهايمر، إلى أن الموافقات على العقاقير الجديدة "علامة فارقة بالنسبة للأشخاص المؤهلين للحصول على هذا العلاج" [2]. وفي الوقت نفسه، كانت عملية الموافقة عليها محاطة بالجدل، خاصةً في حالة Aduhelm [1، 4].
كمريض، ربما تتساءل عن الفرق بين دواء ليكيمبي (ليكانماب) ودواء Aduhelm (أدوكانوماب). في هذه المقالة، سنقارن بين العقارين من حيث طريقة عملهما وفعاليتهما، بالإضافة إلى تكلفتهما وتوفرهما.
ليكيمبي ضد Aduhelm: في ماذا يستخدمون؟
كلا الدواءين علاجان لمرض الزهايمر المبكر. وهما علاجان مضادان للأميلويد ويستهدفان لويحات الأميلويد في الدماغ.
وفقًا لمعلومات وصفاتهما الطبية، فإن ليكيمبي Aduhelm مخصصان للمرضى الذين يعانون من ضعف إدراكي خفيف والذين يعانون من مستويات بيتا أميلويد مرتفعة مؤكدة [5].
ليكيمبي ضد Aduhelm: كيف يعملان؟
أوجه التشابه
ليكيمبي (ليكانماب) Aduhelm (أدوكانوماب) كلاهما أجسام مضادة أحادية النسيلة. وهما مصممان لاستهداف لويحات بيتا أميلويد التي تتراكم في أدمغة مرضى الزهايمر. يُعتقد أن هذه اللويحات تساهم في التدهور المعرفي والتدهور السريري الذي يظهر في هذا المرض.
ويرتبط كلا الدواءين بلويحات الأميلويد ويقومان بتحييدها، بهدف إبطاء تطور المرض. وهذا ما يجعل ليكيمبي Aduhelm مختلفين اختلافًا جوهريًا عن علاجات الزهايمر السابقة مثل جالانتامين وريفاستيجمين ودونيبيزيل. تركز هذه العلاجات السابقة على تخفيف أعراض المرض. يهدف عقارا ليكيمبي Aduhelm إلى تغيير مسار المرض من خلال استهداف سببه الجذري.
الاختلافات
يرتبط ليكيمبي Aduhelm بأجزاء مختلفة من بروتين بيتا أميلويد. يرتبط Aduhelm بقوة أكبر مع لويحات الأميلويد الكبيرة والمتصلبة. وتفيد التقارير أن ليكيمبي يستهدف بشكل أفضل الشكل الأصغر القابل للذوبان (والأكثر سمية) من بروتين الأميلويد [6].
ما مدى كفاءة ليكيمبي Aduhelm
تمت دراسة فعالية ليكيمبي (ليكانماب) Aduhelm(أدوكانوماب) في التجارب السريرية.
-
نتائج تجارب ليكيمبي السريرية
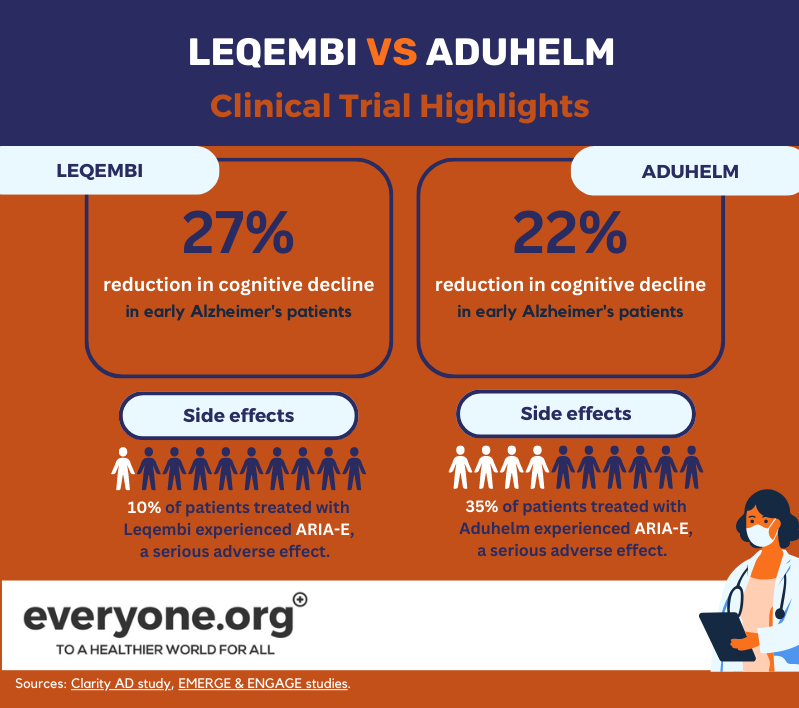
وقد استندت موافقة إدارة الغذاء والدواء الأمريكية على تسريع موافقة إدارة الغذاء والدواء الأمريكية على عقار ليكانماب على النتائج الإيجابية للمرحلة الثالثة من دراسة كلاريتي لمرض الزهايمر. ووفقًا لهذه النتائج، أبطأ عقار ليكانماب من التدهور المعرفي بنسبة تصل إلى 27% لدى مرضى الزهايمر في مراحله المبكرة، مقارنةً بالعلاج الوهمي. تم قياس هذه النتائج بعد 18 شهرًا من بدء العلاج [8].
نُشر تحليل إضافي لنتائج الدراسة في أبريل 2023. وأظهر التحليل أنه حتى بعد توقف المرضى عن تناول ليكيمبي لمدة تتراوح بين 9 إلى 59 شهرًا، استمروا في الاستفادة من تأخير التدهور المعرفي. خلال "فترة الفجوة" هذه، بدا أن مرض الزهايمر يتطور بمعدل أبطأ باستمرار لدى المرضى الذين تلقوا ليكيمبي في التجربة السريرية الأصلية، مقارنةً بالمرضى الذين تلقوا العلاج الوهمي [7].
وحدث التأثير الضار الخطير لـ ARIA-E في 10% من المرضى الذين عولجوا بعقار ليكيمبي. كما عانى 6% من المرضى الذين خضعوا للتجربة من التأثير الضار الخطير لـ ARIA-H، وهو تأثير ضار خطير آخر [13].
-
نتائج تجربة Aduhelm السريرية
وقد منحت إدارة الغذاء والدواء الأمريكية موافقتها المعجّلة لدواء Aduhelm على أساس تجربتين سريريتين للمرحلة الثالثة. أظهرت إحداهما (EMERGE) انخفاضًا في التدهور السريري للمرضى بنسبة تصل إلى 22% [12]. ولم تُظهر الأخرى (ENGAGE) ذلك. ومع ذلك، أظهر Aduhelm في كلتا الدراستين انخفاضًا في لويحات الأميلويد في الدماغ [9]. وقررت إدارة الغذاء والدواء الأمريكية أن هذا المؤشر "من المرجح بشكل معقول أن يؤدي إلى [وجود] فائدة سريرية" [10].
بدأت المرحلة الرابعة من التجربة التأكيديّة (ENVISION) في يونيو 2022، بناءً على طلب إدارة الغذاء والدواء الأمريكية. ومن المتوقع ظهور النتائج في عام 2026 [9].
وفقًا لمعلومات وصفة Aduhelm الطبية، عانى 35% من المرضى الذين يتلقون الدواء في التجارب السريرية من ARIA-E. 34% من مرضى التجارب عانوا من ARIA-H [15].
وكما تُظهر هذه البيانات الحالية، يبدو أن الفرق الرئيسي بين ليكيمبي Aduhelm في هذه المرحلة يكمن في ملف السلامة الخاص بهما، حيث يُظهر ليكيمبي نسبة أقل من الآثار الضارة.
في الوقت نفسه، استنادًا إلى بيانات التجارب السريرية الحالية، يبدو أن دواء ليكيمبي يقدم تأثيرًا أكثر اتساقًا على التدهور المعرفي. ستوفر نتائج التجارب الجارية على كل من ليكيمبي Aduhelm مزيدًا من الوضوح بشأن أداء كلا الدواءين.
ملاحظة: النتائج المعروضة هنا هي لأغراض إعلامية ولا ينبغي استخدامها كأساس لاختيار العلاج. طبيبك هو الأقدر على تحديد العلاج الأنسب لحالتك.

ليكيمبي مقابل Aduhelm: السلامة والآثار الجانبية
وفقًا لمعلومات الوصفة الطبية، هذه هي الآثار الجانبية الأكثر شيوعًا لعقار ليكيمبي (ليكانماب) Aduhelm:
الآثار الجانبية لليكيمبي
- التفاعلات المرتبطة بالتسريب، بما في ذلك الحمى والأعراض الشبيهة بالإنفلونزا والغثيان والتغيرات في معدل السمع وضيق التنفس;
- الصداع;
- التشوهات التصويرية المرتبطة بالأميلويد (ARIA) [13]. قد ينطوي ARIA على تورم مؤقت أو نزيف في الدماغ. تتمثل أعراض ARIA في الصداع والارتباك والنوبات وصعوبة المشي والدوار. قد يكون حاملو جين البروتين الشحمي المتماثل اللواقح E أكثر عرضة لخطر الإصابة بـ ARIA [14].
الآثار الجانبية Aduhelm
الآثار الجانبية الأكثر شيوعًا Aduhelm هي أريا والصداع والسقوط. أحد التفاعلات الضائرة المحددة لـ Aduhelm ولكن ليس لـ Leqembi هو فرط الحساسية. قد تشمل تفاعلات فرط الحساسية الوذمة الوعائية (تورم الطبقات العميقة من الجلد) والأرتكاريا (طفح جلدي) [15].
ليكيمبي مقابل Aduhelm: مقارنة الأسعار
عندما يتعلق الأمر بالأدوية غير المتوفرة على نطاق واسع حتى الآن، يجب أن تأخذ أي سعر كمؤشر فقط. تميل التكاليف النهائية إلى الاختلاف حسب موقعك أو الموردين أو التغطية التأمينية.
لإعطائك فكرة، تكلف قارورة جرعة واحدة من ليكيمبي حوالي 1,043 يورو. مع إعطاء الدواء الموصى به كل أسبوعين، وبذلك تصل التكاليف السنوية لشخص واحد إلى حوالي 27,118 يورو [16].
يبلغ السعر الإرشادي لدواء Aduhelm لكل قارورة جرعة واحدة 1,335 يورو. ومن حيث التكاليف السنوية لشخص واحد، يصل هذا السعر إلى 34,710 يورو [17].
أين تم اعتماد ليكيمبي Aduhelm
تمت الموافقة على عقار ليكيمبي (ليكانيماب) حاليًا في الولايات المتحدة الأمريكية والمملكة المتحدة فقط، ومن المتوقع الحصول على موافقة الاتحاد الأوروبي بحلول نهاية عام 2024[3]. قدم ليكيمبي أيضًا طلبات ترخيص التسويق في الصين واليابان [18، 19، 20].
حصل عقار Aduhelm (aducanumab) على الموافقة المعجّلة من إدارة الغذاء والدواء الأمريكية في الولايات المتحدة الأمريكية في يونيو 2021. رفضت وكالة الأدوية الأوروبية (EMA) طلب تسويق Aduhelm في ديسمبر 2021. تم سحب الطلب لاحقًا من قبل شركة Biogen في أبريل 2022 [21]. كما أرسلت وزارة الصحة اليابانية إشارة سلبية بشأن الموافقة على Aduhelm في البلاد [22].
هل ليكيمبي أو Aduhelm غير معتمدين أو متاحين (حتى الآن) في بلدك؟ إذا كنت ترى أنت وطبيبك أن هذه العلاجات قد تفيدك، فتواصل مع فريقنا من خبراء الوصول إلى الأدوية. يمكننا أن نقدم لك عرض أسعار مخصص للحصول على الدواء من أجلك.
المراجع:
- الجسم المضاد أحادي النسيلة المضاد للأميلويد ليكانماب: 16 ملاحظة تحذيرية. زينودو، 3 يناير 2023.
- هاميلتون، جون إدارة الغذاء والدواء الأمريكية تمنح دواء الزهايمر "ليكيمبي" موافقة معجّلة: لقطات - أخبار الصحة. NPR، 6 يناير 2023.
- اللجنة الاستشارية لإدارة الغذاء والدواء الأمريكية تصوّت بالإجماع على تأكيد الفائدة السريرية لدواء LEQEMBI® (lecanemab-irmb) لعلاج مرض الزهايمر. بيوجين | علاقات المستثمرين، 9 يونيو 2023.
- هيلمور، إدوارد إدارة الغذاء والدواء الأمريكية تتعرض لانتقادات شديدة بسبب الموافقة على عقار Aduhelm لمرض الزهايمر. الجارديان، 29 ديسمبر 2022.
- أبرز معلومات الوصفة الطبية. ليكيمبي، تم الوصول إليه في 3 أغسطس 2023.
- تايلور، إيما. علاج جديد لمرض الزهايمر، ليكانماب، يتصدر عناوين الأخبار: ماذا بعد؟ أبحاث الزهايمر في المملكة المتحدة، 13 ديسمبر 2022.
- إيساي: مرضى الزهايمر يرون فوائد دواء "ليكيمبي" حتى عند إيقافه سي إن بي سي، 6 أبريل 2023
- لقيمبي |الزفوروم. الزفوروم، 30 مايو 2023، تم الوصول إليه في 3 أغسطس 2023.
- Aduhelm |الزفوروم. الزفوروم، 6 فبراير 2023، تم الوصول إليه في 3 أغسطس 2023.
- كافازوني، باتريزيا. قرار إدارة الغذاء والدواء الأمريكية بالموافقة على علاج جديد لمرض الزهايمر. إدارة الغذاء والدواء، 7 يونيو 2021.
- تقدم Eisai النتائج الكاملة من تجربة المرحلة الثالثة من تجربة Clarity AD من ليكانيماب. ألزهايمر أوروبا، 30 نوفمبر 2022.
- النتائج الأولية لدراستي المرحلة الثالثة لتقييم عقار أدوكانوماب في المرضى الذين يعانون من مرض الزهايمر المبكر: دراستان من المرحلة الثالثة لتقييم عقار أدوكانوماب في المرضى الذين يعانون من مرض الزهايمر المبكر. بيوجين |علاقات المستثمرين، تم الوصول إليه في 3 أغسطس 2023.
- المعرف المرجعي: 5105416. Accessdata.fda.gov، تم الوصول إليه في 3 أغسطس 2023.
- الدليل الدوائي حقنة ليكيمبي® (leqEMBI®) (ليكانماب-إيرمب)، للاستخدام الوريدي. ليكيمبي، تم الوصول إليه في 3 أغسطس 2023.
- أبرز معلومات الوصفات الطبية. Accessdata.fda.gov، تم الوصول إليه في 3 أغسطس 2023.
- اشتر ليكيمبي (lecanemab-irmb) عبر الإنترنت - السعر والتكاليف. Everyone.org تم الوصول إليه في 3 أغسطس 2023.
- اشتر Aduhelm (aducanumab-avwa) عبر الإنترنت - السعر والتكاليف. Everyone.org تم الوصول إليه في 3 أغسطس 2023.
- شركة EISAI تقدم طلب ترخيص تسويق عقار LECANEMAB كعلاج لمرض الزهايمر المبكر في أوروبا | Biogen. بيوجين |علاقات المستثمرين، 10 يناير 2023.
- إيساي تشرع في تقديم بيانات اتفاقية ترخيص إطلاق السجل التجاري (BLA) لـ Lecanemab في الصين | Biogen. Biogen |علاقات المستثمرين، 22 ديسمبر 2022.
- كارفالهو، تيريزا، وراي بورو. ليكانماب، لمرض الزهايمر المبكر قيد المراجعة في اليابان. أخبار الزهايمر اليوم، 14 مارس 2022.
- تحديث بشأن التقديم التنظيمي لعقار أدوكانوماب في الاتحاد الأوروبي | Biogen. Biogen | علاقات المستثمرين، 22 أبريل 2022.
- سويفت، روكي وآخرون. عقار إيساي-بيوجين للزهايمر يصعب تقييمه - وزارة الصحة اليابانية. رويترز، 22 ديسمبر 2021.